कैल्शियम बाइकार्बोनेट संरचना, गुण, जोखिम और उपयोग
कैल्शियम बाइकार्बोनेट रासायनिक सूत्र Ca (HCO) के साथ अकार्बनिक नमक है3)2. यह प्रकृति में कैल्शियम कार्बोनेट से चूना पत्थर की चट्टानों और कैल्सिट जैसे खनिजों में मौजूद है.
कैल्शियम कार्बोनेट की तुलना में कैल्शियम बाइकार्बोनेट पानी में अधिक घुलनशील है। इस विशेषता ने चूना पत्थर की चट्टानों में और गुफाओं की संरचना में करास्ट सिस्टम के निर्माण की अनुमति दी है.

दरार से गुजरने वाले भूमिगत जल कार्बन डाइऑक्साइड (CO) के विस्थापन में संतृप्त हो जाते हैं2)। ये जल कैल्शियम कार्बोनेट (CaCO) को छोड़ने वाले चूना पत्थर की चट्टानों को नष्ट कर देते हैं3) जो निम्न प्रतिक्रिया के अनुसार कैल्शियम बाइकार्बोनेट का निर्माण करेगा:
CaCO3(s) + CO2(g) + एच2O (l) => Ca (HCO)3)2(AQ)
यह प्रतिक्रिया उन गुफाओं में होती है जहां बहुत कठोर पानी की उत्पत्ति होती है। कैल्सियम के साथ कैल्शियम बाइकार्बोनेट ठोस अवस्था में नहीं बल्कि एक जलीय घोल में पाया जाता है2+, बाइकार्बोनेट (HCO)3-) और कार्बोनेट आयन (CO)32-).
इसके बाद, जब पानी में कार्बन डाइऑक्साइड की संतृप्ति कम हो जाती है, तो रिवर्स प्रतिक्रिया होती है, यह कहना है कैल्शियम कार्बोनेट में कैल्शियम बाइकार्बोनेट के परिवर्तन का:
सीए (HCO)3)2(aq) => CO2 (g) + एच2O (l) + CaCO3 (एस)
कैल्शियम कार्बोनेट पानी में खराब रूप से घुलनशील है, इससे इसकी वर्षा ठोस के रूप में होती है। उपर्युक्त प्रतिक्रिया गुफाओं में स्टैलेक्टाइट्स, स्टैलेग्माइट्स और अन्य स्पेलोथेथम्स के गठन में बहुत महत्वपूर्ण है.
ये चट्टानी संरचनाएं पानी की बूंदों से बनती हैं जो गुफाओं (शीर्ष छवि) की छत से गिरती हैं। सीएसीओ3 उल्लिखित संरचनाओं को बनाने के लिए पानी की बूंदों में मौजूद क्रिस्टलीकरण किया जाता है.
तथ्य यह है कि ठोस अवस्था में कैल्शियम बाइकार्बोनेट नहीं पाया जाता है, इसके उपयोग को कठिन बना दिया है, और कुछ उदाहरण पाए जाते हैं। साथ ही, इसके विषैले प्रभावों के बारे में जानकारी प्राप्त करना मुश्किल है। ऑस्टियोपोरोसिस को रोकने के लिए उपचार के रूप में इसके उपयोग के दुष्प्रभावों के एक सेट की रिपोर्ट है.
संरचना
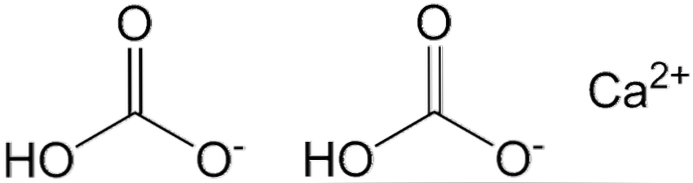
ऊपरी छवि में दो HCO आयनों को दिखाया गया है3- और एक कैशन2+ इलेक्ट्रोस्टिक रूप से बातचीत करना। द सी2+ छवि के अनुसार, यह बीच में स्थित होना चाहिए, क्योंकि यह एचसीओ कैसे है3- वे अपने नकारात्मक आरोपों के कारण एक-दूसरे को पीछे नहीं हटाएंगे.
HCO में नकारात्मक चार्ज3- सी = ओ कार्बोनिल समूह और सी-ओ बांड के बीच प्रतिध्वनि द्वारा इसे दो ऑक्सीजन परमाणुओं के बीच में विभाजित किया गया है-; जबकि सीओ में32-, यह तीन ऑक्सीजन परमाणुओं के बीच में विभाजित है, क्योंकि सी-ओएच बंधन का विघटन होता है और इसलिए प्रतिध्वनि के लिए ऋणात्मक आवेश प्राप्त कर सकता है.
इन आयनों की ज्यामिति को हाइड्रोजनीकृत अंत के साथ कार्बोनेट के फ्लैट त्रिकोण से घिरे कैल्शियम के क्षेत्र के रूप में माना जा सकता है। आकार के अनुपात के संदर्भ में, कैल्शियम एचसीओ आयनों की तुलना में काफी छोटा है3-.
जलीय घोल
द सीए (HCO)3)2 यह क्रिस्टलीय ठोस नहीं बना सकता है, और इसमें वास्तव में इस नमक के जलीय घोल होते हैं। उनमें, आयन अकेले नहीं हैं, जैसा कि छवि में है, लेकिन एच अणुओं से घिरा हुआ है।2हे.
वे कैसे बातचीत करते हैं? प्रत्येक आयन एक जलयोजन क्षेत्र से घिरा हुआ है, जो धातु, ध्रुवीयता और भंग प्रजातियों की संरचना पर निर्भर करेगा.
द सी2+ जल के ऑक्सीजन परमाणुओं के साथ निर्देशांक बनाने के लिए एक जलकोशिका, Ca (OH)2)n2+, जहाँ n को आम तौर पर छह माना जाता है; वह है, कैल्शियम के आसपास एक "जलीय ऑक्टाहेड्रॉन".
जबकि HCO आयनों3- या तो हाइड्रोजन बांड के साथ बातचीत (या2सीओ-एच-OH2) या नकारात्मक चार्ज डेलोकॉलाइज़ (HOCO) की दिशा में पानी में हाइड्रोजन परमाणुओं के साथ2- एच-ओएच, डिपोल-आयन इंटरैक्शन).
सीए के बीच ये बातचीत2+, HCO3- और पानी इतना कुशल है, कि वे उस विलायक में कैल्शियम बाइकार्बोनेट को बहुत घुलनशील बनाते हैं; CCO के विपरीत3, जिसमें Ca के बीच इलेक्ट्रोस्टैटिक आकर्षण है2+ और सीओ32- बहुत मजबूत होते हैं, जलीय घोल से अवक्षेपित होते हैं.
पानी के अलावा, सीओ अणु होते हैं2 आसपास, जो अधिक एचसीओ प्रदान करने के लिए धीरे-धीरे प्रतिक्रिया करता है3- (पीएच मान के आधार पर).
हाइपोथेटिकल ठोस
अब तक, Ca (HCO) में आयनों के आकार और प्रभार3)2, न ही पानी की उपस्थिति, समझाएं कि ठोस यौगिक मौजूद क्यों नहीं है; वह है, शुद्ध क्रिस्टल जिन्हें एक्स-रे क्रिस्टलोग्राफी द्वारा चित्रित किया जा सकता है। Ca (HCO)3)2 पानी में मौजूद आयनों से अधिक कुछ भी नहीं है, जहां से खौफनाक मंजर बढ़ते रहते हैं.
हां कै2+ और एचसीओ3- उन्हें निम्नलिखित रासायनिक प्रतिक्रिया से बचने वाले पानी से अलग किया जा सकता है:
सीए (HCO)3)2(aq) → काको3(s) + CO2(g) + एच2ओ (एल)
तब इन्हें एक सफेद क्रिस्टलीय ठोस में रखा जा सकता है जिसमें स्टोइकोमीट्रिक अनुपात 2: 1 (2HCO) होता है3/ 1 सी ए)। इसकी संरचना के बारे में कोई अध्ययन नहीं हैं, लेकिन इसकी तुलना NaHCO के साथ की जा सकती है3 (मैग्नीशियम बाइकार्बोनेट के लिए, Mg (HCO)3)2, न तो ठोस के रूप में मौजूद है), या काको के साथ3.
स्थिरता: NaHCO3 बनाम सीए (HCO)3)2
नाहको3 मोनोक्लिनिक प्रणाली, और CaCO में क्रिस्टलीकृत होता है3 त्रिकोणीय (केल्साइट) और ऑर्थोरोम्बिक (एरेगोनाइट) प्रणालियों में। अगर ना को बदल दिया जाता+ सीए के लिए2+, आकार में अधिक अंतर से क्रिस्टलीय नेटवर्क को अस्थिर किया जाएगा; वह है, ना+ क्योंकि यह छोटा है, यह HCO के साथ अधिक स्थिर क्रिस्टल बनाता है3- सीए की तुलना में2+.
वास्तव में, सीए (HCO)3)2(aq) पानी को वाष्पीकृत करने की आवश्यकता होती है ताकि उसके आयनों को एक क्रिस्टल में समूहीकृत किया जा सके; लेकिन इस एक के क्रिस्टल जाली कमरे के तापमान पर ऐसा करने के लिए पर्याप्त मजबूत नहीं है। जब पानी गर्म होता है, तो अपघटन प्रतिक्रिया होती है (ऊपर समीकरण).
ना आयन होना+ समाधान में, यह HCO के साथ क्रिस्टल का निर्माण करेगा3- थर्मल अपघटन से पहले.
इसके बाद सीए (HCO) क्यों3)2 यह क्रिस्टलीकृत नहीं होता (सैद्धांतिक रूप से), यह आयनिक रेडीआई या इसके आयनों के आकार के अंतर से होता है, जो अपघटन से पहले एक स्थिर क्रिस्टल नहीं बना सकता है.
सीए (HCO)3)2 बनाम काको3
अगर दूसरी तरफ, एच जोड़ा गया था+ CCO के क्रिस्टलीय संरचनाओं के लिए3, वे अपने भौतिक गुणों को काफी बदल देंगे। शायद, इसके पिघलने के बिंदु स्पष्ट रूप से गिरते हैं, और यहां तक कि, क्रिस्टल की आकृति विज्ञान भी संशोधित होते हैं.
क्या यह Ca (HCO) के संश्लेषण की कोशिश करने लायक होगा3)2 ठोस? कठिनाइयाँ अपेक्षाओं को पार कर सकती हैं, और कम संरचनात्मक स्थिरता वाला एक नमक किसी भी अनुप्रयोग में महत्वपूर्ण अतिरिक्त लाभ प्रदान नहीं कर सकता है जहां अन्य लवण पहले से ही उपयोग किए जाते हैं.
भौतिक और रासायनिक गुण
रासायनिक सूत्र
सीए (HCO)3)2
आणविक भार
162.11 ग्राम / मोल
भौतिक अवस्था
यह ठोस अवस्था में दिखाई नहीं देता है। यह जलीय घोल में पाया जाता है और पानी के वाष्पीकरण द्वारा इसे ठोस में बदलने का प्रयास करता है, इसने कैल्शियम कार्बोनेट में परिवर्तित होने पर काम नहीं किया है।.
पानी में घुलनशीलता
0 डिग्री सेल्सियस पर 16.1 ग्राम / 100 मिलीलीटर; 20 डिग्री सेल्सियस पर 16.6 ग्राम / 100 मिलीलीटर और 100 डिग्री सेल्सियस पर 18.4 ग्राम / 100 मिलीलीटर। ये मान सीए आयनों (एचसीओ) के लिए पानी के अणुओं की उच्च आत्मीयता का संकेत हैं।3)2, जैसा कि पिछले भाग में बताया गया है। इस बीच, केवल 15 मिलीग्राम सीएसीओ है3 वे एक लीटर पानी में घुलते हैं, जो उनके मजबूत इलेक्ट्रोस्टैटिक इंटरैक्शन को दर्शाता है.
क्योंकि सीए (HCO)3)2 यह एक ठोस नहीं बना सकता है, इसकी घुलनशीलता को प्रयोगात्मक रूप से निर्धारित नहीं किया जा सकता है। हालांकि, सीओ द्वारा बनाई गई शर्तों को देखते हुए2 चूना पत्थर के आसपास के पानी में भंग, एक तापमान T पर भंग कैल्शियम के द्रव्यमान की गणना की जा सकती है; द्रव्यमान, जो Ca (HCO) की सांद्रता के बराबर होगा3)2.
अलग-अलग तापमानों पर, 0, 20 और 100 ° C पर मानों के अनुसार विघटित द्रव्यमान बढ़ता है। तो, इन प्रयोगों के अनुसार, सीए (एचसीओ) का कितना निर्धारण किया जाता है3)2 काको के आसपास के क्षेत्र में घुल जाता है3 सीओ के साथ एक जलीय माध्यम में गैसीफाइड2. एक बार सीओ भाग निकले2 गैसीय, CaCO3 वेग होगा, लेकिन सीए (HCO) नहीं3)2.
फ्यूजन और क्वथनांक
Ca (HCO) का क्रिस्टलीय नेटवर्क3)2 काको की तुलना में बहुत कमजोर है3. यदि यह एक ठोस अवस्था में प्राप्त किया जा सकता है, और उस तापमान को मापता है जिस पर यह फुसियोमीटर के अंदर पिघलता है, तो यह निश्चित रूप से 899ºC के नीचे एक मूल्य प्राप्त करेगा। इसी तरह, उबलते बिंदु के निर्धारण में भी उम्मीद की जा सकती है.
दहन बिंदु
यह दहनशील नहीं है.
जोखिम
चूंकि यह यौगिक ठोस रूप में मौजूद नहीं है, इसलिए यह संभावना नहीं है कि यह दोनों जलीय समाधानों में हेरफेर करने के लिए एक जोखिम का प्रतिनिधित्व करेगा, क्योंकि दोनों सीए2+ HCO के रूप में3- वे कम सांद्रता में हानिकारक नहीं हैं; और इसलिए, सबसे बड़ा जोखिम जो इस तरह के समाधानों को प्राप्त करना होगा, केवल कैल्शियम की एक खतरनाक खुराक के कारण हो सकता है.
यदि यौगिक एक ठोस का गठन करता है, भले ही यह सीएसीओ से शारीरिक रूप से भिन्न हो3, इसके विषैले प्रभाव शारीरिक संपर्क या साँस लेने के बाद साधारण परेशानी और बचाव से परे नहीं जा सकते हैं.
अनुप्रयोगों
-कैल्शियम बाइकार्बोनेट समाधानों का उपयोग लंबे समय से पुराने कागजों को धोने के लिए किया जाता है, विशेष रूप से कला या ऐतिहासिक रूप से महत्वपूर्ण दस्तावेजों का काम करता है.
-बाइकार्बोनेट समाधान का उपयोग उपयोगी है, न केवल क्योंकि वे कागज में एसिड को बेअसर करते हैं, बल्कि कैल्शियम कार्बोनेट का एक क्षारीय आरक्षित भी प्रदान करते हैं। यह अंतिम यौगिक कागज पर भविष्य के नुकसान के लिए सुरक्षा प्रदान करता है.
-अन्य बिकारबोनिट की तरह, इसका उपयोग रासायनिक खमीर में और अपशिष्ट गोलियों या पाउडर के निर्माण में किया जाता है। इसके अलावा, कैल्शियम बाइकार्बोनेट का उपयोग खाद्य योज्य (इस नमक के जलीय घोल) के रूप में किया जाता है।.
-ऑस्टियोपोरोसिस की रोकथाम में बाइकार्बोनेट समाधान का उपयोग किया गया है। हालांकि, एक मामले में हाइपरलकसीमिया, मेटाबॉलिक अल्कलोसिस और गुर्दे की विफलता जैसे माध्यमिक प्रभाव देखे गए हैं।.
-कैल्शियम बाइकार्बोनेट को कभी-कभी, हृदय क्रिया के लिए हाइपोकैलिमिया के अवसादग्रस्तता प्रभाव को ठीक करने के लिए प्रशासित किया जाता है।.
-और अंत में, यह शरीर को कैल्शियम प्रदान करता है, जो मांसपेशियों के संकुचन का एक मध्यस्थ है, उसी समय यह एसिडोसिस को ठीक करता है जो हाइपोकैलेमिया की स्थिति में हो सकता है।.
संदर्भ
- विकिपीडिया। (2018)। कैल्शियम बाइकार्बोनेट। से लिया गया: en.wikipedia.org
- सिराह डुबोइस। (3 अक्टूबर, 2017)। कैल्शियम बाइकार्बोनेट क्या है? से लिया गया: livestrong.com
- विज्ञान सीखना हब। (2018)। कार्बोनेट रसायन। से लिया गया: Sciencelearn.org.nz
- PubChem। (2018)। कैल्शियम बाइकार्बोनेट। से लिया गया: pubchem.ncbi.nlm.nih.gov
- एमी ई। गेरब्रा और आइरीन ब्रुकल। (1997)। लघु संरक्षण कार्यशालाओं में कैल्शियम बाइकार्बोनेट और मैग्नीशियम बाइकार्बोनेट समाधान का उपयोग: सर्वेक्षण परिणाम। से लिया गया: cool.conservation-us.org


