एथिल एसीटेट संरचना, गुण, संश्लेषण, उपयोग और जोखिम
एथिल एसीटेट या एथिल एथानोएट (आईयूपीएसी नाम) एक कार्बनिक यौगिक है जिसका रासायनिक सूत्र सीएच है3COOC2एच5. इसमें एक एस्टर होता है, जहां अल्कोहल घटक इथेनॉल से निकलता है, जबकि इसका कार्बोक्जिलिक एसिड घटक एसिटिक एसिड से आता है.
यह तापमान और दबाव की सामान्य परिस्थितियों में एक तरल है, जो फलों को सुखद सुगंध प्रदान करता है। यह संपत्ति पूरी तरह से सद्भाव में प्रवेश करती है जो एस्टर से अपेक्षित है; जो वास्तव में एथिल एसीटेट की रासायनिक प्रकृति है। इस कारण से यह खाद्य उत्पादों और मादक पेय पदार्थों में उपयोग पाता है.
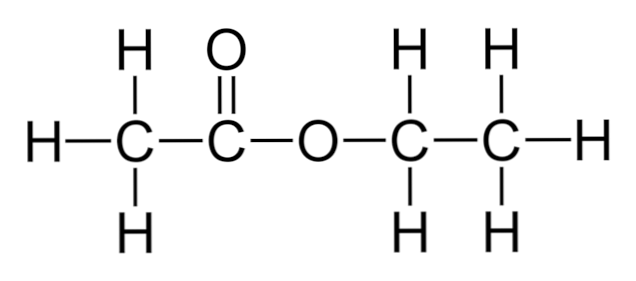
ऊपरी छवि में, एथिल एसीटेट की संरचना कंकाल को दिखाया गया है। बाईं ओर इसके कार्बोक्जिलिक एसिड घटक, और शराब घटक के दाईं ओर ध्यान दें। संरचनात्मक दृष्टिकोण से, यह उम्मीद की जा सकती है कि यह यौगिक सिरका और शराब के बीच एक संकर की तरह व्यवहार करता है; हालाँकि, यह स्वयं के गुणों को प्रदर्शित करता है.
यह वह जगह है जहां एस्टर नाम की ऐसी हाइब्रिड अलग-अलग होती है। एथिल एसीटेट एक एसिड के रूप में प्रतिक्रिया नहीं कर सकता है, और न ही यह ओएच समूह की अनुपस्थिति में निर्जलीकरण कर सकता है। इसके बजाय, यह एक मजबूत आधार की उपस्थिति में बुनियादी हाइड्रोलिसिस से गुजरता है, जैसे कि सोडियम हाइड्रॉक्साइड, NaOH.
इस हाइड्रोलिसिस प्रतिक्रिया का उपयोग रासायनिक गतिज प्रयोगों के लिए प्रयोगशालाओं को पढ़ाने में किया जाता है; जहां प्रतिक्रिया, इसके अलावा, दूसरे क्रम की है। जब हाइड्रोलिसिस होता है, तो व्यावहारिक रूप से इथाइल एथानोएट अपने प्रारंभिक घटकों में लौटता है: एसिड (NaOH द्वारा अवक्षेपित) और शराब.
इसकी संरचनात्मक कंकाल में यह देखा गया है कि हाइड्रोजन परमाणु ऑक्सीजन के ऊपर प्रबल होते हैं। यह गैर-ध्रुवीय प्रजातियों जैसे वसा के साथ बातचीत करने की उनकी क्षमता को प्रभावित करता है। यह भी रेजिन, रंजक और सामान्य कार्बनिक ठोस जैसे यौगिकों को भंग करने के लिए उपयोग किया जाता है.
एक सुखद सुगंध होने के बावजूद, इस तरल के लंबे समय तक संपर्क शरीर में एक नकारात्मक प्रभाव (लगभग सभी रासायनिक यौगिकों की तरह) उत्पन्न करता है.
सूची
- 1 एथिल एसीटेट की संरचना
- 1.1 हाइड्रोजन दाता परमाणुओं की अनुपस्थिति
- 2 भौतिक और रासायनिक गुण
- २.१ नाम
- २.२ आणविक सूत्र
- 2.3 आणविक भार
- २.४ शारीरिक वर्णन
- 2.5 रंग
- 2.6 गंध
- 2.7 स्वाद
- 2.8 गंध सीमा
- 2.9 क्वथनांक
- 2.10 गलनांक
- 2.11 पानी में घुलनशीलता
- 2.12 कार्बनिक सॉल्वैंट्स में घुलनशीलता
- 2.13 घनत्व
- 2.14 वाष्प घनत्व
- 2.15 स्थिरता
- 2.16 वाष्प दाब
- 2.17 चिपचिपापन
- 2.18 दहन की गर्मी
- 2.19 वाष्पीकरण गर्मी
- 2.20 सतह तनाव
- 2.21 अपवर्तक सूचकांक
- 2.22 भंडारण तापमान
- 2.23 पीकेए
- 3 सारांश
- 3.1 फिशर की प्रतिक्रिया
- 3.2 Tishchenko प्रतिक्रिया
- ३.३ अन्य विधियाँ
- 4 उपयोग
- 4.1 सॉल्वेंट
- ४.२ कृत्रिम स्वाद
- 4.3 विश्लेषिकी
- 4.4 कार्बनिक संश्लेषण
- 4.5 क्रोमैटोग्राफी
- 4.6 एंटोमोलॉजी
- 5 जोखिम
- 6 संदर्भ
एथिल एसीटेट की संरचना
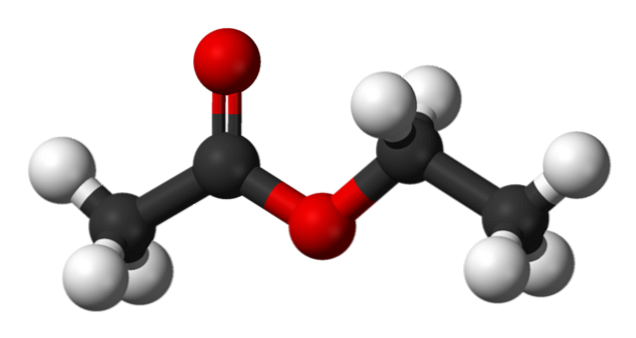
ऊपरी छवि में एथिल एसीटेट की संरचना को गोले और बार के मॉडल के साथ दिखाया गया है। इस मॉडल में लाल क्षेत्रों के साथ ऑक्सीजन परमाणुओं पर प्रकाश डाला गया है; इसके बाईं ओर एसिड से प्राप्त अंश है, और इसके दाईं ओर अल्कोहल (एल्कोक्सी समूह, -OR) से प्राप्त अंश है.
कार्बोनिल समूह को सी = ओ बांड (डबल बार) द्वारा सराहना की जाती है। इस समूह और आसन्न ऑक्सीजन के आस-पास की संरचना समतल है, क्योंकि दोनों ऑक्सीजेंस के बीच प्रतिध्वनि द्वारा भार का एक विकेन्द्रीकरण होता है; तथ्य यह है कि α-hydrogens (-CH समूह के) की अपेक्षाकृत कम अम्लता की व्याख्या करता है3, C = O से जुड़ा हुआ.
अणु, अपने दो बंधों को घुमाकर, सीधे इस बात का पक्ष लेता है कि यह अन्य अणुओं के साथ कैसे संपर्क करता है। दो ऑक्सीजन परमाणुओं की उपस्थिति, और संरचना में विषमता, इसे एक स्थायी द्विध्रुवीय क्षण दें; जो, बदले में, उनके द्विध्रुवीय-द्विध्रुवीय अंतःक्रियाओं के लिए जिम्मेदार है.
उदाहरण के लिए, इलेक्ट्रॉनिक घनत्व दो ऑक्सीजन परमाणुओं के पास अधिक होता है, समूह -CH में काफी कम हो जाता है3, और धीरे-धीरे OCH समूह में2सीएच3.
इन इंटरैक्शन के कारण, एथिल एसीटेट अणु सामान्य परिस्थितियों में एक तरल बनाते हैं, जिसमें काफी उच्च क्वथनांक (77 ,T) होता है।.
हाइड्रोजन बांड के दाता परमाणुओं की अनुपस्थिति
यदि आप संरचना को करीब से देखते हैं, तो आप हाइड्रोजन पुल को दान करने में सक्षम परमाणु की अनुपस्थिति को नोटिस करेंगे। हालांकि, ऑक्सीजन परमाणु ऐसे स्वीकारकर्ता हैं, और एथिल एसीटेट पानी में बहुत घुलनशील है, और ध्रुवीय यौगिकों और हाइड्रोजन बांड दाताओं (जैसे शक्कर) के साथ एक प्रशंसनीय डिग्री के लिए बातचीत करता है।.
इसके अलावा, यह आपको इथेनॉल के साथ उत्कृष्ट रूप से बातचीत करने की अनुमति देता है; जिसके कारण मादक पेय पदार्थों में इसकी उपस्थिति आश्चर्यजनक नहीं है.
दूसरी ओर, इसका एल्कोक्सी समूह इसे कुछ एपोलर यौगिकों, जैसे क्लोरोफॉर्म, सीएच के साथ बातचीत करने में सक्षम बनाता है3क्लोरीन.
भौतिक और रासायनिक गुण
नाम
-एथिल एसीटेट
-एथिल एथानोएट
-एसिटिक एसिड एस्टर
-Acetoxietano
आणविक सूत्र
सी4एच8हे2 या सी.एच.3COOC2एच5
आणविक भार
88,106 ग्राम / मोल.
शारीरिक विवरण
साफ रंगहीन तरल.
रंग
रंगहीन तरल.
गंध
पंखों की विशेषता, अनानास की गंध के समान.
स्वाद
पतला होने पर सुखद, बियर में फल स्वाद जोड़ता है.
गंध दहलीज
3.9 पीपीएम। 0.0196 मिलीग्राम / मी3 (कम गंध); 665 मिलीग्राम / मी3 (उच्च गंध).
7 पर पता लगाने योग्य गंध - 50 पीपीएम (मतलब = 8 पीपीएम).
क्वथनांक
171 ° F से 760 mmHg (77.1 ° C).
गलनांक
-118.5 (F (-83.8 ºC).
पानी में घुलनशीलता
80 ग्राम / एल.
कार्बनिक सॉल्वैंट्स में घुलनशीलता
इथेनॉल और एथिल ईथर के साथ गलतफहमी। एसीटोन और बेंजीन में बहुत घुलनशील। क्लोरोफॉर्म, फिक्स्ड और वाष्पशील तेलों के साथ और ऑक्सीजन युक्त और क्लोरीनयुक्त सॉल्वैंट्स के साथ भी कुरूप.
घनत्व
0.9003 ग्राम / सेमी3.
वाष्प का घनत्व
3.04 (वायु अनुपात में: 1).
स्थिरता
यह नमी के साथ धीरे-धीरे विघटित होता है; कई प्लास्टिक और मजबूत ऑक्सीकरण एजेंटों के साथ असंगत। पानी के साथ मिश्रण विस्फोटक हो सकता है.
भाप का दबाव
25.2C पर 93.2 mmHg
चिपचिपापन
2523 ise पर 0.423 mPoise.
दहन की गर्मी
2,238.1 केजे / मोल.
वाष्पीकरण गर्मी
25 kC पर 35.60 kJ / मोल.
सतह तनाव
२० .C पर २४ डायन / सेमी.
अपवर्तनांक
2037। सी / डी पर 1,373.
भंडारण तापमान
2 - 8 - सी.
pKa
16 - 18 25 ºC पर.
संश्लेषण
फिशर की प्रतिक्रिया
एथिल एसीटेट को फ़िशर प्रतिक्रिया द्वारा औद्योगिक रूप से संश्लेषित किया जाता है, जिसमें एथेनॉल एसिटिक एसिड के साथ एस्टराइज़र होता है। प्रतिक्रिया कमरे के तापमान पर की जाती है.
सीएच3सीएच2ओह + सीएच3COOH <=> सीएच3COOCH2सीएच3 + एच2हे
एसिड उत्प्रेरक द्वारा प्रतिक्रिया को तेज किया जाता है। संतुलन सही करने के लिए चलता है, अर्थात्, पानी को हटाने के माध्यम से एथिल एसीटेट के उत्पादन की ओर; जन कार्रवाई के कानून के अनुसार.
Tishchenko की प्रतिक्रिया
एथिल एसीटेट को टिशेंको प्रतिक्रिया का उपयोग करके औद्योगिक रूप से भी तैयार किया जाता है, एक उत्प्रेरक के रूप में एल्कोऑक्साइड के उपयोग के साथ एसिटालडिहाइड के दो समकक्षों को मिलाता है।.
2 सीएच3CHO => CH3COOCH2सीएच3
अन्य विधियाँ
-175 डिग्री सेल्सियस और 50 एटीएम दबाव के तापमान पर किए गए एक प्रतिक्रिया में एथिल एसीटेट को ब्यूटेन के ऑक्सीकरण में एक प्रतिदीप्ति के रूप में संश्लेषित किया जाता है। कोबाल्ट और क्रोमियम आयनों को उत्प्रेरक के रूप में उपयोग किया जाता है.
-एथिल एसीटेट पॉलीविनाइल एसीटेट से पॉलीविनाइल अल्कोहल के इथेनॉलिसिस का एक प्रतिरूप है.
-एथिल एसीटेट का उत्पादन उद्योग में इथेनॉल के डिहाइड्रोजनेशन द्वारा भी किया जाता है, जो एक ऊंचे तापमान पर तांबे के उपयोग से उत्प्रेरित होता है, लेकिन 250 ° C से कम होता है।.
अनुप्रयोगों
विलायक
एथिल एसीटेट का उपयोग विलायक और मंदक के रूप में किया जाता है, जिसका उपयोग सर्किट बोर्डों की सफाई में किया जाता है। यह संशोधित हॉप निकालने के निर्माण में, और कॉफी और चाय की पत्तियों के डिकैफ़िनेशन में एक विलायक के रूप में उपयोग किया जाता है। इसका उपयोग फलों और सब्जियों को चिह्नित करने के लिए उपयोग की जाने वाली स्याही में किया जाता है.
एथिल एसीटेट का उपयोग कपड़ा उद्योग में सफाई एजेंट के रूप में किया जाता है। इसका उपयोग थर्मामीटर के अंशांकन में किया जाता है, जिसका उपयोग शर्करा के पृथक्करण में किया जाता है। पेंट उद्योग में इसका उपयोग सामग्रियों के विलायक और मंदक के रूप में किया जाता है.
कृत्रिम स्वाद
इसका उपयोग फलों के स्वाद के विस्तार में किया जाता है; उदाहरण के लिए: केला, नाशपाती, आड़ू और अनानास, साथ ही अंगूर की सुगंध आदि।.
विश्लेषणात्मक
इसका उपयोग बिस्मथ, बोरॉन, सोना, मोलिब्डेनम और प्लैटिनम के निर्धारण के साथ-साथ थैलियम विलायक के निर्धारण में किया जाता है। एथिल एसीटेट में जलीय घोल में मौजूद कई यौगिकों और तत्वों को निकालने की क्षमता होती है, जैसे: फास्फोरस, कोबाल्ट, टंगस्टन और आर्सेनिक.
कार्बनिक संश्लेषण
एथिल एसीटेट का उपयोग उद्योग में फोटोसिस्टिस्ट योगों में उपयोग किए जाने वाले रेजिन के लिए एक चिपचिपापन reducer के रूप में किया जाता है। इसका उपयोग एसिटामाइड, एसिटाइल एसीटेट और मिथाइल हेप्टानोन के उत्पादन में किया जाता है.
क्रोमैटोग्राफी
प्रयोगशालाओं में, एथिल एसीटेट का उपयोग स्तंभ क्रोमैटोग्राफी के मोबाइल चरण और निष्कर्षण विलायक के रूप में किया जाता है। एथिल एसीटेट को अपेक्षाकृत कम क्वथनांक होने से, वाष्पित करना आसान होता है, जो विलायक में घुले पदार्थों को केंद्रित करने की अनुमति देता है.
कीटविज्ञान
एथिल एसीटेट का उपयोग एंटोमोलॉजी में एक कंटेनर में रखे जाने वाले कीटों को करने के लिए किया जाता है, जो इसके संग्रह और अध्ययन की अनुमति देता है। एथिल एसीटेट के वाष्प कीट को नष्ट किए बिना उसे नष्ट कर देते हैं और इसके सख्त होने से रोकते हैं, संग्रह के लिए इसकी विधानसभा को सुविधाजनक बनाते हैं.
जोखिम
-एलडी50 चूहों में एथिल एसीटेट कम विषाक्तता को इंगित करता है। हालांकि, यह त्वचा, आंखों, त्वचा, नाक और गले में जलन कर सकता है.
-उच्च स्तर के संपर्क में आने से चक्कर आना और बेहोशी हो सकती है। साथ ही, लंबे समय तक एक्सपोज़र लिवर और किडनी को प्रभावित कर सकता है.
-20,000 की एकाग्रता में एथिल एसीटेट की साँस लेना - 43,000 पीपीएम के कारण फुफ्फुसीय एडिमा और रक्तस्राव हो सकता है.
-व्यावसायिक जोखिम की सीमा OSHA द्वारा हवा में 400 पीपीएम पर निर्धारित की गई है, औसतन, 8 घंटे के काम के दौरान.
संदर्भ
- स्टीवन ए। हार्डिंगर। (2017)। ऑर्गेनिक केमिस्ट्री की सचित्र शब्दावली: एथिल एसीटेट (EtOAc)। से लिया गया: chem.ucla.edu
- ग्राहम सोलोमन्स टी। डब्ल्यू।, क्रेग बी। फ्राइले। (2011)। कार्बनिक रसायन। Amines। (10वें संस्करण।)। विली प्लस.
- मॉरिसन, आर.टी. एंड बॉयड, आर.एन. (1990)। कार्बनिक रसायन (5टा संस्करण)। संपादकीय एडिसन-वेस्ले इबोरामेरिकाना.
- विकिपीडिया। (2019)। एथिल एसीटेट। से लिया गया: en.wikipedia.org
- कपास एस। (S.f.)। एथिल एसीटेट। से लिया गया: chm.bris.ac.uk
- PubChem। (2019)। एथिल एसीटेट। से लिया गया: pubchem.ncbi.nlm.nih.gov
- न्यूसेड केमिकल। (2018)। एथिल एसीटेट के अनुप्रयोग और उपयोग। से लिया गया: foodsweeteners.com
- वरिष्ठ सेवाओं के स्वास्थ्य के न्यू जर्सी विभाग। (2002)। एथिल एसीटेट। [PDF]। से लिया गया: nj.gov


