सोडियम क्लोराइड (NaCl) संरचना, गुण, उपयोग, विषाक्तता
सोडियम क्लोराइड, जिसे आम नमक या टेबल सॉल्ट भी कहा जाता है, क्षार धातु सोडियम और हैलोजन क्लोरीन का एक द्विआधारी अकार्बनिक नमक है। यह खाद्य नमक का सबसे बड़ा घटक है और इसके खनिज रूप को हैलाइट के रूप में जाना जाता है। इसका आणविक सूत्र NaCl है, और इसके आयनों (Na) के स्टोइकोमेट्रिक अनुपात का वर्णन करता है+ क्लोरीन-) और असतत अणु का नहीं (Na-Cl)
सोडियम क्लोराइड एक क्रिस्टलीय सफेद ठोस है जो सोडियम, सिलवरी सफेद धातु के संयोजन से बनता है, जो पानी के साथ हिंसक प्रतिक्रिया करता है, और क्लोरीन तत्व, एक जहरीला, संक्षारक, हल्का हरा गैस.

ऊपरी छवि में NaCl क्रिस्टल का एक भाग दिखाया गया है। यह कैसे संभव है कि दो तत्व Na और Cl जितना खतरनाक हो2, क्या एक खाद्य नमक बनाया जा सकता है? सबसे पहले, इसके गठन के लिए रासायनिक समीकरण है:
2Na (s) + सीएल2(g) => 2NaCl (s)
उत्तर NaCl में लिंक की प्रकृति में निहित है। आयनिक होने के नाते, ना के गुण+ और सीएल- वे अपने तटस्थ परमाणुओं से तिरछे अलग हैं.
सोडियम एक महत्वपूर्ण तत्व है, लेकिन इसके आयनिक रूप में। ना+ लगभग 140 mEq / lt की एकाग्रता के साथ मुख्य बाह्य कोशिकीकरण है, और साथ में इसके आयनों, Cl- और एचसीओ3- (बाइकार्बोनेट), मुख्य रूप से ऑस्मोलैरिटी और बाह्यकोशिका के मूल्य के लिए जिम्मेदार हैं.
इसके अलावा, ना+ न्यूरोनल एक्सोन में तंत्रिका आवेगों की पीढ़ी और प्रवाहकत्त्व के साथ-साथ मांसपेशियों के संकुचन की शुरुआत के लिए जिम्मेदार है.
भोजन को स्वाद देने और मांस को संरक्षित करने, बैक्टीरिया को खत्म करने और खराब होने से बचाने के लिए NaCl का उपयोग प्राचीन काल से किया जाता रहा है.
यह सोडियम हाइड्रॉक्साइड (NaOH) और आणविक क्लोरीन (Cl) के उत्पादन के लिए भी आवश्यक है2), हाइड्रोलिसिस के तहत पानी के साथ NaCl प्रतिक्रिया करके:
2H2O (l) + 2 NaCl (s) => 2NaOH (ac) + Cl2(g) + एच2(G)
कैथोड में (-) H जमा होता है2 (छ) और NaOH। इस बीच, एनोड (+) पर Cl जम जाता है2 (G)। सोडियम हाइड्रॉक्साइड का उपयोग पीवीसी प्लास्टिक के निर्माण में साबुन और क्लोरीन के निर्माण में किया जाता है.
सूची
- 1 सोडियम क्लोराइड की संरचना
- 1.1 एकात्मक प्रकोष्ठ
- 2 गुण
- २.१ आणविक सूत्र
- २.२ आणविक भार
- २.३ शारीरिक विवरण
- २.४ रंग
- 2.5 स्वाद
- 2.6 क्वथनांक
- 2.7 गलनांक
- 2.8 पानी में घुलनशीलता
- 2.9 कार्बनिक सॉल्वैंट्स में घुलनशीलता
- 2.10 घनत्व
- 2.11 वाष्प दाब
- 2.12 स्थिरता
- 2.13 अपघटन
- 2.14 चिपचिपापन
- 2.15 जंग
- 2.16 पीएच
- ३ उपयोग
- ३.१ भोजन में
- 3.2 औद्योगिक उपयोग
- 3.3 घर पर
- ३.४ अन्य उपयोग
- 3.5 चिकित्सीय उपयोग
- 4 विषाक्तता
- 4.1 अंतर्ग्रहण
- ४.२ जलन और शारीरिक संपर्क
- 5 संदर्भ
सोडियम क्लोराइड की संरचना
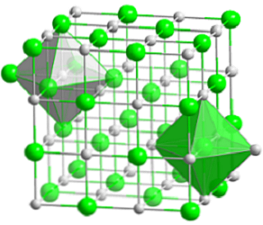
ऊपरी छवि में सोडियम क्लोराइड की कॉम्पैक्ट क्यूबिक संरचना का प्रतिनिधित्व किया गया है। हरे हरे रंग के गोले Cl anions के अनुरूप हैं-, सफेद करने के लिए, ना cations के लिए+. ध्यान दें कि कैसे NaCl क्रिस्टल में 1: 1 अनुपात में उनके इलेक्ट्रोस्टैटिक इंटरैक्शन द्वारा व्यवस्थित आयनों का एक नेटवर्क होता है.
हालाँकि छवि में बार दिखाए जाते हैं, बॉन्ड सहसंयोजक नहीं होते हैं लेकिन आयनिक होते हैं। आयन के चारों ओर समन्वय ज्यामिति दिखाते समय सलाखों का उपयोग उपयोगी होता है। उदाहरण के लिए, NaCl प्रत्येक Na के मामले में+ छह सीएल से घिरा हुआ है- (सफेद ऑक्टाहेड्रोन), और प्रत्येक सीएल- छह ना का+ (हरा ऑक्टाहेड्रॉन).
इसलिए, इसमें एक समन्वय (6,6) है जिनकी संख्या इंगित करती है कि कितने पड़ोसी प्रत्येक आयन को घेरे हुए हैं। दाईं ओर की संख्या Na के पड़ोसियों को इंगित करती है+, जबकि बाईं ओर एक, सीएल-.
अन्य अभ्यावेदन संरचना के पास मौजूद अष्टकोणीय छिद्रों को उजागर करने के लिए सलाखों के उपयोग को छोड़ देते हैं, जिसके परिणामस्वरूप छह सीएल आयनों के बीच के बीच का स्थान होता है।- (या ना+) पैक किया हुआ। यह व्यवस्था अन्य मोनो (एमएक्स) या पॉलीआटोमिक अकार्बनिक लवणों में देखी जाती है, और इसे रत्न नमक कहा जाता है।.
एकात्मक कोशिका
सेंधा नमक की इकाई कोशिका क्यूबिक है, लेकिन कौन सा क्यूब्स वास्तव में ऊपर की छवि में इसका प्रतिनिधित्व करता है? अष्टद्रव्य उत्तर देते हैं। दोनों कुल चार छोटे क्यूब्स को कवर करते हैं.
इन क्यूब्स में आयनों के भाग उनके कोने, किनारों और चेहरों में होते हैं। ध्यान से देखा जाए तो एक आयन ना+ यह केंद्र में स्थित है और किनारों में उनमें से बारह है। एक किनारे पर एक आयन चार क्यूब्स द्वारा साझा किया जा सकता है। तो 4 ना आयन हैं+ (१२ × १/४ + १ = ४).
सीएल आयनों के लिए-, आठ कोने में स्थित हैं और किनारों में छह हैं। चूंकि कोने पर स्थित आयन आठ अन्य क्यूब्स के साथ अंतरिक्ष साझा करते हैं, और छह के साथ किनारों पर, उनके पास 4 क्लियन हैं- (8 × 1/8 + 6 × 1/2 = 4).
पिछले परिणाम की व्याख्या निम्नानुसार की जाती है: NaCl की इकाई कोशिका में चार Na संकेतन होते हैं+ और चार सीएल आयनों-; अनुपात जो रासायनिक सूत्र (एक ना) से मेल खाता है+ प्रत्येक सीएल के लिए-).
गुण
आणविक सूत्र
सोडियम क्लोराइड.
आणविक भार
58.44 ग्राम / मोल.
शारीरिक विवरण
एक क्रिस्टलीय ठोस.
रंग
पारदर्शी रंगहीन क्रिस्टल या सफेद क्रिस्टलीय पाउडर.
स्वाद
नमकीन.
क्वथनांक
2,575 5F से 760 mmHg.
1,465 4C है.
गलनांक
1,474 47F (800,7 4C).
क्वथनांक और गलनांक दोनों ही क्रिस्टलीय जालीदार ऊर्जा को दूर करने के लिए आवश्यक ऊष्मा को दर्शाते हैं। इसलिए, ये माप NaCl के आयनिक वर्ण की पुष्टि करते हैं.
पानी में घुलनशीलता
68 ° F पर 100 mg / ml से अधिक या बराबर.
25 डिग्री सेल्सियस पर 36.0 ग्राम / 100 मिली.
यह वास्तव में एक हीड्रोस्कोपिक नमक है, जो पर्यावरण से नमी को बरकरार रखता है.
कार्बनिक सॉल्वैंट्स में घुलनशीलता
25 डिग्री सेल्सियस पर इथेनॉल के 0.065 ग्राम / 100 एमएल; 25 डिग्री सेल्सियस पर ग्लिसरॉल के 10 ग्राम / 100 ग्राम; 40 डिग्री सेल्सियस पर 2.15 ग्राम / 100 एमएल तरल अमोनियम; 25 डिग्री सेल्सियस पर मेथनॉल के 1.4 ग्राम / 100 एमएल; 25 डिग्री सेल्सियस पर इथाइलीन ग्लाइकॉल के 7.15 ग्राम / 100 और 25 डिग्री सेल्सियस पर फॉर्मिक एसिड के 5.21 ग्राम / 100 ग्राम.
घनत्व
2,165 ग्राम / सेमी3 77 º सी पर.
भाप का दबाव
1 mmHg से 1,589 1,F.
स्थिरता
यह अनुशंसित भंडारण स्थितियों के तहत स्थिर है.
सड़न
उच्च तापमान पर गर्म होने पर यह हाइड्रोक्लोरिक एसिड और डिसोडियम ऑक्साइड के वाष्प का उत्सर्जन करता है.
चिपचिपापन
संतृप्त समाधानों की चिपचिपाहट 1.93 mPa-s.
जंग
यह कई धातुओं के लिए संक्षारक है.
पीएच
जलीय घोल में 6.7 से 7.3.
अनुप्रयोगों
भोजन में
-सोडियम क्लोराइड का उपयोग प्राचीन काल से भोजन के स्वाद और इसके संरक्षण में सुधार के लिए किया जाता रहा है। मांस का नमकीन बनाना बैक्टीरिया की कार्रवाई से इसे संरक्षित करने का एक तरीका है, क्योंकि यह प्रोटीन अपघटन में देरी करता है.
-दूसरी ओर, नमक मांस के चारों ओर परासरण को बढ़ाता है, जो बैक्टीरिया के पानी के परासरण द्वारा अवशोषण का कारण बनता है जो इसके उन्मूलन का कारण बनता है.
औद्योगिक उपयोग करता है
खाद्य उद्योग
-खाद्य उद्योग में, नमक का उपयोग स्वाद बढ़ाने, किण्वन नियंत्रण योजक, बनावट नियंत्रण एजेंट और रंग डेवलपर के रूप में किया जाता है। उदाहरण के लिए, बेकन, हैम और अन्य मांस उत्पादों में रंग को उजागर करने के लिए नमक जोड़ा जाता है.
-सॉसेज के निर्माण में नमक एक बांधने की मशीन के रूप में कार्य करता है। यह मांस, वसा और नमी से बने बाइंडर जेल के निर्माण में योगदान देता है.
-रोटी बनाने के लिए आटा के प्रसंस्करण में, रोटी के आटे के किण्वन की दर को नियंत्रित करने के लिए खाना पकाने के दौरान नमक जोड़ा जाता है। इसका उपयोग लस को मजबूत करने और स्वाद बढ़ाने के साथ-साथ पके हुए माल को भरने के लिए भी किया जाता है.
-इसका उपयोग नाश्ते के अनाज, मिश्रित या तैयार आटा, फ्रेंच फ्राइज़, कुत्तों और बिल्लियों के भोजन, आदि के निर्माण में किया जाता है।.
रासायनिक उत्पादों का संश्लेषण
-सोडियम क्लोराइड का उपयोग सोडियम हाइड्रॉक्साइड और क्लोरीन के उत्पादन में कच्चे माल के रूप में किया जाता है, जो कई रासायनिक उद्योगों में उपयोगी होता है।.
-नमक का उपयोग विभिन्न धातुओं के प्रसंस्करण में किया जाता है, उदाहरण के लिए एल्यूमीनियम, तांबा, स्टील और वैनेडियम। इसका उपयोग सोडियम क्लोरेट करने के लिए भी किया जाता है, जो बाद में क्लोरीन डाइऑक्साइड, ऑक्सीजन-आधारित ब्लीच के संश्लेषण में उपयोग किया जाता है। अन्य ब्लीच की तुलना में क्लोरीन डाइऑक्साइड पर्यावरण के लिए कम हानिकारक है.
चमड़ा उद्योग में
-नमक का उपयोग खाल के अंदर बैक्टीरिया की क्रिया को रोकने के लिए किया जाता है, साथ ही इसके पुनर्जलीकरण में भी मदद करता है.
कपड़ा उद्योग में
-कपड़ों की रंगाई में नमक का इस्तेमाल मॉर्डन के रूप में किया जाता है। इसका उपयोग कार्बनिक संदूकों को हटाने और कपड़े की सतह पर सकारात्मक चार्ज बनाने के लिए एक नमकीन कुल्ला के रूप में किया जाता है जो नकारात्मक रूप से चार्ज किए गए रंगों के संघ की अनुमति देता है.
तेल उद्योग में
-तेल और गैस की खोज में, नमक अच्छी तरह से ड्रिलिंग तरल पदार्थ का एक महत्वपूर्ण घटक है। इसका उपयोग ड्रिलिंग तरल पदार्थ के घनत्व को फ्लोक्युलेट करने और बढ़ाने के लिए किया जाता है, जो उन कुओं में गैस के उच्च दबावों को दूर करने की अनुमति देता है जिन्हें पहुंचना है। इसके अलावा, नमक ड्रिलिंग तरल की संतृप्ति को बनाए रखता है.
-नमक उस मिट्टी को कॉम्पैक्ट करने में मदद करता है जिस पर सड़कें बनी हैं। नमी और ऑटोमोटिव ट्रैफ़िक में बदलाव से उप-मौसम में होने वाले विस्थापन को कम करता है.
घर पर
नमक का उपयोग सतहों, बर्तनों और धूपदान की सफाई में रगड़ कर किया गया है। मोल्ड की रोकथाम में और दाग हटानेवाला के रूप में भी। इसके अलावा, यह कई ब्रांडों के शैम्पू और टूथपेस्ट में उपयोग किया जाता है.
अन्य उपयोग
सड़कों पर
-बर्फबारी के अनुमान में सड़कें नमकीन पानी से ढँक जाती हैं, जिससे सड़क की सतह पर बर्फ का जमाव रुक जाता है। विगलन के लिए, नमकीन और नमक के मिश्रण का उपयोग किया जाता है, और अन्य रासायनिक घटकों जैसे मैग्नीशियम या कैल्शियम क्लोराइड को कभी-कभी जोड़ा जाता है। -10 .C से नीचे के तापमान पर नमक और नमकीन का उपयोग प्रभावी नहीं है.
नमक जोड़ते समय, क्रायोस्कोपिक बिंदु में कमी होती है, समाधानों की एक संपीड़ित संपत्ति होती है, जो बर्फ के गठन में किसी तरह से बाधा डालती है.
-इसकी हीड्रोस्कोपिक स्थिति के कारण, नमक का उपयोग सस्ते डेसिस्केंट के रूप में किया जाता है.
पानी नरम करने के लिए उपयोग किए जाने वाले रेजिन में
कठोर पानी में कैल्शियम और मैग्नीशियम आयन होते हैं जो साबुन की क्रिया में बाधा डालते हैं और विभिन्न उपकरणों और पाइपों में क्षारीय पदार्थों के जमा का उत्पादन करते हैं। पानी के नरम होने में, आयन एक्सचेंज रेजिन का उपयोग किया जाता है। नमक का उपयोग रेजिन की तैयारी और पुनर्जनन में किया जाता है.
आग बुझाने पर
आग बुझाने के लिए सोडियम क्लोराइड का उपयोग आग बुझाने में किया जाता है जिसमें दहनशील धातुएं मौजूद होती हैं, जैसे कि मैग्नीशियम, पोटेशियम, सोडियम और एनके मिश्र.
नमक एक हीट सिंक के रूप में और एक कोल्हू के रूप में कार्य करता है जो आग में ऑक्सीजन की पहुंच को प्रतिबंधित करता है.
चश्मे में
सोडियम क्लोराइड क्रिस्टल का उपयोग ऑप्टिकल घटकों में किया जाता है जैसे कि खिड़कियां और प्रिज्म, विशेष रूप से अवरक्त प्रकाश के लिए। हालांकि, चूंकि नमक बहुत हीड्रोस्कोपिक है, इसलिए एक प्रकार का ठंढ होता है जो लेंस को कवर करता है। इस कारण से, सोडियम क्लोराइड लेंस को जिंक सेलेनाइड (ZnSe) से बदल दिया गया है.
चिकित्सीय उपयोग
शरीर में लवण की कमी को पूरा करने के लिए
-जब ना का शरीर क्षीण होता है+, बाह्य परासरण, तंत्रिका चालन और मांसपेशियों के संकुचन को बनाए रखने के लिए प्रतिस्थापित किया जाना चाहिए.
-NaCl का उपयोग सोडियम और क्लोरीन की कमी के उपचार और रोकथाम में किया जाता है, जिसके परिणामस्वरूप उच्च तापमान के संपर्क में अधिक पसीना आता है। इसका उपयोग अत्यधिक डायरिया या नमक के अधिक सेवन पर प्रतिबंध में किया जाता है.
-एक 045% NaCl समाधान के पैरेन्टेरियल डिलीवरी का उपयोग हाइपरोस्मोलर मधुमेह के प्रबंधन में किया जाता है। यह एक पुनर्जलीकरण कार्य को पूरा करता है और गुर्दे समारोह की स्थिति का मूल्यांकन करने के लिए कार्य करता है.
-हाइपरटोनिक समाधान के इंजेक्शन, NaCl एकाग्रता 0.9% w / v से अधिक के साथ,
-उनका उपयोग तब किया जाता है जब कोई गंभीर कमी न हो+, आवश्यक आयन की बहाली होने के नाते। यह हाइपोनेट्रेमिया मुक्त इलेक्ट्रोलाइट्स के साथ या ना की एकाग्रता के साथ उपचार का परिणाम हो सकता है+.
हाइपोनेट्रेमिया अत्यधिक पानी के सेवन के कारण भी हो सकता है, अपर्याप्त गुर्दे समारोह द्वारा नियंत्रित नहीं किया जाता है.
उपचार और अपरंपरागत उपयोगों में
-नेब्यूलेशन प्रक्रिया के दौरान उपयोग की जाने वाली दवाओं को पतला करने के लिए NaCl इनहेलेशन समाधानों का उपयोग किया जाता है। इसका उपयोग ट्रेकिअल धुलाई और सिंचाई के लिए भी किया जाता है। नाक स्प्रे में इस्तेमाल 0.9% खारा समाधान.
-20% NaCl समाधान का उपयोग इंट्रा-एमनियोटिक ट्रांसबॉम्बो इंस्टॉलेशन के लिए किया जाता है, इस प्रकार गर्भावस्था के दूसरे ट्रांसफर के दौरान देर से गर्भपात के लिए प्रेरित किया जाता है.
-सोडियम क्लोराइड का उपयोग स्थानीय एंटीसेप्टिक के रूप में किया जा सकता है। इसकी आसमाटिक क्षमता के लिए धन्यवाद यह एक असंतुलित अवस्था में वायरस और बैक्टीरिया के व्यापक स्पेक्ट्रम को निर्जलित करने में सक्षम है; इसलिए, यह घावों कीटाणुरहित करने के लिए एक दर्दनाक एंटीसेप्टिक के रूप में उपयोग किया जाता है.
विषाक्तता
घूस
यदि इसका सेवन अधिक और लंबे समय तक किया जाए तो इसका स्वास्थ्य पर हानिकारक प्रभाव पड़ता है। इन परिस्थितियों में अतिरक्तदाब अतिरिक्त मात्रा में परिणामी वृद्धि के साथ होता है जो उच्च रक्तचाप को जन्म देगा.
जलन और शारीरिक संपर्क
यह एक विषाक्त प्रभाव है केवल अगर साँस लेना बहुत अधिक है। अत्यधिक रूप में त्वचा के संपर्क में आने से इसकी शुष्कता हो सकती है। अंत में, यह आंखों के संपर्क में क्षणिक जलन पैदा करता है.
संदर्भ
- कंपकंपी और एटकिंस। (2008)। अकार्बनिक रसायन (चौथा संस्करण, पेज 84, 90, 93, 263)। मैक ग्रे हिल.
- Whitten, डेविस, पेक और स्टेनली। रसायन विज्ञान। (8 वां संस्करण।) काँगेज लर्निंग, पी 482-483.
- सोडियम क्लोराइड (2018)। सोडियम क्लोराइड: लाभ, उपयोग, गुण, जोखिम। से लिया गया: clorurodesodio.org
- PubChem। (2018)। सोडियम क्लोराइड। से लिया गया: pubchem.ncbi.nlm.nih.gov
- विकिपीडिया। (2018)। सोडियम क्लोराइड। से लिया गया: en.wikipedia.org
- अमेरिकी तत्व। (2018)। सोडियम क्लोराइड। से लिया गया: americanelements.com


